
Los perros afectados suelen presentar hinchazón y eritema del tejido epitelial del conducto auditivo externo, aumento de la secreción de las glándulas ceruminosas del oído, sacudidas de cabeza y comportamientos que sugieren dolor y prurito óticos. La otitis externa puede deberse a varias causas; en la mayoría de los casos crónicos, existe más de una causa. Las causas primarias de la otitis externa incluyen infecciones parasitarias, cuerpos extraños, neoplasias, trastornos de hipersensibilidad, trastornos de la queratinización, enfermedades glandulares y enfermedades autoinmunes. Algunos perros pueden estar predispuestos a padecer otitis externa si tienen conductos auditivos anormalmente pequeños o restrictivos, orejas colgantes, humedad excesiva en el oído o sufren traumatismos en el oído.
Las bacterias y las levaduras rara vez son causas primarias, y suelen considerarse importantes factores perpetuadores. Staphylococcus pseudintermedius, Pseudomonas aeruginosa, Proteus spp, Escherichia coli y Klebsiella spp son los patógenos secundarios más comúnmente aislados. Malassezia pachydermatis es la levadura más común que contribuye a la otitis externa como factor perpetuante. El diagnóstico se realiza fácilmente a partir de la anamnesis y la exploración física. El examen citológico y/o el cultivo son valiosos para determinar qué agentes infecciosos están presentes, si los hay. El tratamiento de la otitis externa depende de la identificación y el control de las enfermedades predisponentes y primarias siempre que sea posible. Además, la limpieza de los conductos auditivos, la aplicación de terapias tópicas y la administración de medicamentos sistémicos pueden ser necesarias para la eliminación y el control eficaces de las causas primarias y los factores perpetuantes.
El miconazol es un derivado sintético del imidazol con una elevada actividad antifúngica y una fuerte actividad contra bacterias Gram-positivas como S. aureus, Miconazol ha demostrado eficacia in vitro e in vivo en perros contra varias especies de levaduras, entre ellas M. pachydermatis aislado de casos de otitis externa canina.
La polimixina B es un antibiótico polipéptido de amplio espectro. Su espectro de actividad consiste predominantemente en bacilos Gram negativos como E. coli, Salmonella, Shigella, y especialmente P. aeruginosa. La aparición de resistencias es rara ya que se utiliza en formulaciones tópicas y no hay reabsorción sistémica. Además, su uso sistémico en veterinaria es escaso o nulo, lo que reduce la posibilidad de desarrollo de cepas resistentes. Por lo tanto, la polimixina B se considera un antibiótico de primera línea en los tratamientos tópicos del oído.
Una característica única de la combinación de polimixina B y miconazol es el efecto sinérgico demostrado contra E. coli, S. aureus, P. aeruginosa y S. aureus. La prednisolona es un glucocorticoide con una fuerte actividad antiinflamatoria y efectos mínimos sobre el metabolismo de carbohidratos y minerales. Dentro del producto de ensayo, sus propiedades antiinflamatorias y antipruriginosas contribuyen a un rápido alivio sintomático y favorecen una rápida curación clínica al disminuir la formación de edema y la dilatación capilar.
Se reclutaron casos clínicos caninos de otitis externa en clínicas veterinarias de animales de compañía de cuatro zonas geográficas de Estados Unidos y Canadá. Cuarenta y nueve investigadores de 31 clínicas veterinarias participaron en el ensayo. Los perros en buen estado de salud general podían participar en el estudio independientemente de su raza, sexo o edad si presentaban signos clínicos definidos de otitis externa unilateral o bilateral e infección bacteriana y/o por hongos confirmada. Para evaluar la elegibilidad, se realizó una anamnesis y un examen clínico detallados. Se realizó una exploración puntuando el investigador la gravedad de cuatro signos de inflamación del oído: dolor/malestar, eritema, hinchazón y cantidad de exudado del oído.
Se utilizó el siguiente sistema de puntuación: 0 = normal, 1 = leve, 2 =moderado y 3 = marcado. Antes del primer tratamiento se realizó en la clínica veterinaria una limpieza de los oídos para eliminar el material ceroso, los exudados y otros residuos de los pabellones auriculares y de los conductos auditivos del paciente. Como solución limpiadora se utilizó solución salina caliente no permitiendose ningún otro producto de limpieza. En caso necesario, se permitió sedar al animal para facilitar el procedimiento de limpieza y minimizar las molestias.
Este ensayo de campo multicéntrico se llevó a cabo siguiendo las directrices de las Buenas Prácticas Clínicas (VICH GL9) y fue un estudio aleatorizado, doble ciego con un control positivo. Los perros fueron asignados aleatoriamente al producto de prueba que contenía 23 mg de nitrato de miconazol, 0,5293 mg de sulfato de polimixina B y 5 mg de acetato de prednisolona por ml o al producto de control positivo que contenía 10 mg de clotrimazol, 3 mg de sulfato de gentamicina y 1 mg de valerato de betametasona por gramo.
Los perros asignados al azar al grupo del producto de prueba fueron tratados dos veces al día durante 7 días con cinco gotas del producto de prueba. Los perros asignados al azar en el grupo de control positivo fueron tratados dos veces al día durante 7 días con cuatro (perros < 13,6 kg) u ocho (perros ≥ 13,6 kg) gotas. El técnico cualificado del hospital administró el tratamiento inicial. A partir de entonces, todos los demás tratamientos fueron aplicados por el propietario del animal. Por lo tanto, el investigador no tenía conocimiento del tratamiento que había recibido cada perro. No se permitió la administración de ningún antibiótico sistémico o tópico y/o antiinflamatorio distinto del producto de prueba o de control positivo durante el estudio.
Antes de iniciar el tratamiento, y entre 2 y 4 días después de finalizarlo, el investigador realizó un examen físico del perro, en el que se evaluó la gravedad de la otitis. Se puntuó la inflamación (sistema de puntuación descrito anteriormente) y se observó cualquier anomalía clínica del animal. Este examen del oído se realizó antes de cualquier procedimiento de recogida de hisopos o limpieza del oído. En caso de otitis externa bilateral, se eligió el oído derecho, a menos que la puntuación clínica total no sumara 5, en cuyo caso se eligió el oído izquierdo. El investigador también evaluó la audición del perro, se utilizó un silbato audible de alta frecuencia. La evaluación se realizó antes de manipular o examinar físicamente al perro. La audición del perro se clasificó como normal, reducida o ausente. El investigador, en colaboración con el propietario del animal, supervisó cualquier efecto adverso del producto de ensayo y de control positivo.
En la visita inicial se tomó una muestra del oído objeto de la investigación y se examinó microscópicamente en la clínica en busca de ácaros del oído. Se tomó una segunda muestra para análisis de laboratorio, incluido el cultivo de bacterias y levaduras, la identificación y la susceptibilidad antimicrobiana.
Los patógenos identificados, según la evaluación del laboratorio, fueron sometidos a pruebas de susceptibilidad. Los cultivos bacterianos se sometieron a un panel de susceptibilidad que incluía sulfato de polimixina B, sulfato de gentamicina y nitrato de miconazol.
Todos los análisis se realizaron con el programa Sta- tistical Analysis System for Personal Com- puters (SAS) Versión 9.1.3 (SAS Institute, Cary, NC, EE.UU.). La unidad experimental para la evaluación de la eficacia fue una oreja de un perro individual y para la evaluación de la seguridad un perro individual.
Se analizaron dos resultados de los cuatro parámetros clínicos y el parámetro clínico global: el resultado binario «mejoría frente a no mejoría» y el resultado continuo «cambio en la puntuación clínica tras el tratamiento».
La mejoría se definió como una disminución de al menos un nivel en la escala entre el periodo anterior y posterior al tratamiento. En caso contrario, se clasificó como sin mejoría. Para el resultado binario, se ajustó un modelo lineal generalizado con el enlace logit (tratamiento e infección por Staphylococcus spp incluidos como efectos fijos y clínica y tratamiento por clínica como efectos aleatorios) para realizar la prueba de no inferioridad. Se llegó a la conclusión de no inferioridad si el límite inferior del intervalo de confianza unilateral del 95 % para la diferencia de probabilidad de mejora (producto de prueba – producto de control positivo) no fue superior a -10%.
Se incluyeron en el estudio 337 casos clínicos, que iniciaron el tratamiento. La eliminación de casos debida a la violación de los criterios de inclusión/exclusión, al incumplimiento del requisito de crecimiento microbiano o a otras violaciones del protocolo, dio como resultado 176 casos (91 productos de prueba y 85 controles positivos) que cumplían estrictamente el protocolo y, por lo tanto, se consideraron válidos para los análisis de eficacia. Trescientos veinte dos (322) casos para la evaluación de seguridad.
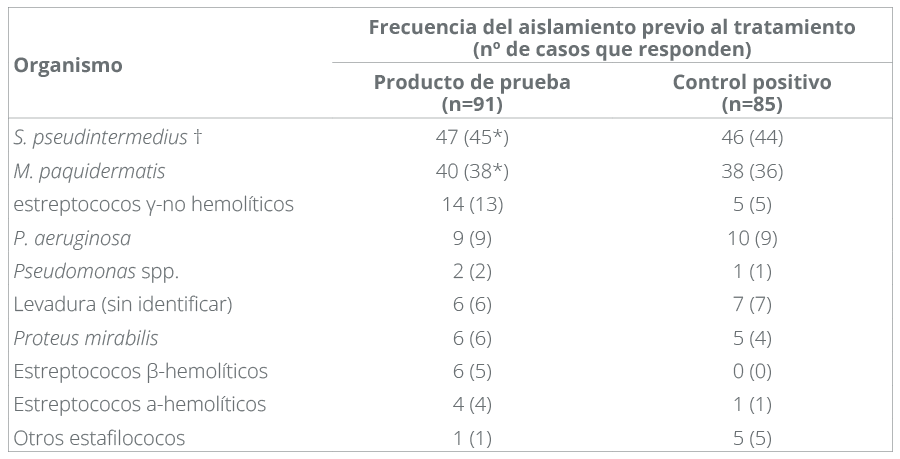
La gran mayoría de los casos de otitis externa de este estudio mostraron una mejoría clínica de los síntomas inflamatorios del oído, con una mejoría clínica del 97% de los casos tratados con el producto de prueba y del 95% de los casos tratados con el producto de control positivo (Tabla 1).
Para el parámetro clínico global, que consideraba los cuatro parámetros clínicos (dolor/malestar, eritema, hinchazón y exudados), y para tres de los cuatro parámetros clínicos por separado (dolor/malestar, eritema y exudados), la proporción media de mejora para la prueba fue superior a la del producto de control positivo. El intervalo de confianza inferior unilateral del 95% de la diferencia de proporción de mejora (producto de prueba – producto de control positivo) no fue menos negativo que -10 % para los cuatro parámetros clínicos y el parámetro clínico global. Así pues, se demostró que el producto de ensayo no era inferior al producto de control positivo.
Además, el producto de ensayo resultó ser superior al producto de control positivo en los parámetros: dolor/malestar, eritema, exudados y el parámetro clínico global.
En cuanto al grado de mejora clínica, en promedio, la puntuación clínica global (dolor, eritema, inflamación y exudados; cada parámetro se calificó de 0 a 3 en gravedad) había disminuido 5,6 puntos para el producto de prueba y 5,5 puntos para el producto de control positivo en el momento de la visita final en comparación con la visita inicial. No hubo diferencias estadísticamente significativas entre los grupos de tratamiento. En más del 80 % de los animales, la puntuación clínica total disminuyó 4 puntos o más.
Los resultados de los frotis auriculares demostraron a menudo la presencia de más de un microorganismo patógeno en cada espécimen. Las especies aisladas con mayor frecuencia fueron S. pseudintermedius y M. pachydermatis. De estos datos se desprende claramente que el producto de ensayo es muy eficaz contra todos los microorganismos aislados, incluidos Staphylococcus spp, Streptococcus spp, Malassezia spp y Pseudomonas spp.
Los aislados bacterianos y de Malassezia fueron sometidos a pruebas de resistencia/sensibilidad a la polimixina B, el miconazol y la gentamicina. Los resultados de las pruebas de susceptibilidad (Tabla 2) demostraron una alta susceptibilidad de M. paquidermatis, S. pseudintermedius, y P. aeruginosa a los componentes activos del producto de ensayo. Ningún perro presentaba aislados de Staphylococcus resistentes a la polimixina B y al miconazol ni aislados de Malassezia resistentes al miconazol. El 60% de los perros tratados con el producto de control positivo tenían cepas de Streptococcus resistentes a la gentamicina, mientras que sólo el 11% de los perros tratados con el producto de prueba tenían cepas de Streptococcus resistentes a la polimixina B y al miconazol. El 30% de los perros tratados con el producto de control positivo presentaban cepas de Pseudomonas resistentes a la gentamicina, mientras que sólo el 9% de los perros tratados con el producto de prueba presentaban cepas de Pseudomonas resistentes a la polimixina B y al miconazol.
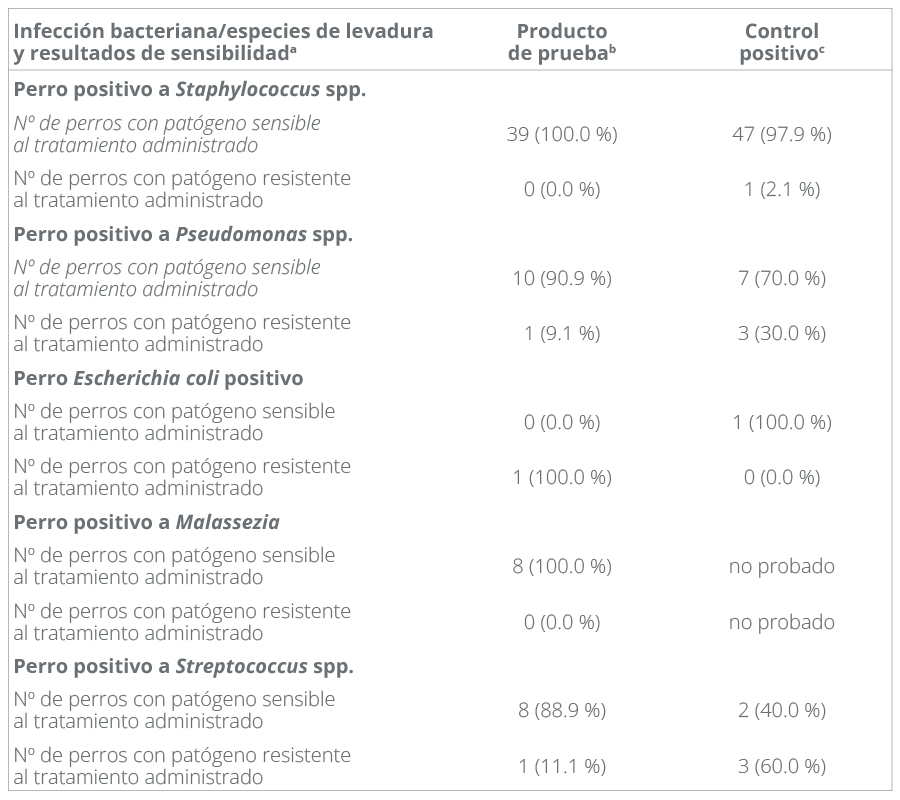
Si en la oreja de un perro había más de una especie del mismo patógeno y si un patógeno se clasificaba como resistente, el perro se clasificaba como resistente independientemente del estatus del otro patógeno.
b Sensible al producto de ensayo = tratamiento con el producto de ensayo + sensible a la polimixina B o al miconazol; resistente al producto de ensayo = tratamiento con el producto de ensayo + resistente a la polimixina B y al miconazol.
c Sensible al control positivo = tratamiento con control positivo + sensible a la gentamicina; resistente al control positivo = tratamiento con control positivo + resistente a la gentamicina.
Los pacientes caninos con inflamación del epitelio del conducto auditivo externo se ven con frecuencia en la práctica veterinaria. La mayoría de los casos de otitis externa en perros responden bien al tratamiento con medicación tópica. Los productos combinados óticos contienen antibióticos, antifúngicos y antiinflamatorios para aliviar las molestias, disminuir la inflamación y, al mismo tiempo, eliminar la infección en el conducto auditivo externo.
Este amplio estudio de campo estadounidense con 337 casos clínicos inscritos de otitis canina externa demostró una mejoría clínica tras el tratamiento auditivo con el producto de ensayo en un oído limpio y a la dosis recomendada aplicado dos veces al día durante 7 días consecutivos.
El producto de ensayo demostró ser eficaz en el 97% de todos los casos clínicos de otitis presentados, con una mejora independiente del animal, peso (raza), sexo, edad y geografía. La mejora clínica de la otitis externa fue mejor para el producto de prueba en comparación con el producto de control positivo en este estudio. El producto de prueba no fue inferior al producto de control positivo en los cuatro parámetros clínicos (dolor/malestar, hinchazón, eritema, exudado) y en el parámetro clínico global.
Un estudio clínico previo se realizó en Australia en el que se comparaba el producto de ensayo con dos productos óticos: uno que contenía neomicina, tiostreptón, nistatina y triamcinolona y otro producto ótico que contenía neomicina, monosulfiram y betametasona. Este estudio demostró que el producto de prueba daba mejores resultados en el tratamiento de la otitis externa canina que ambos productos de control positivo. Con el producto de prueba, se requirió un tratamiento más corto para lograr la recuperación clínica y hubo una menor tasa de recaída en comparación con los otros dos productos.
En este estudio realizado en EE.UU., se recogieron muestras con hisopos de oído de casos clínicos, independientemente de la historia previa de problemas de oído. Los aislamientos determinaron la flora patógena de perros con otitis externa atendidos en la práctica general. Las infecciones mixtas eran frecuentes. Los organismos patógenos cultivados eran Gram positivos, y el 56% de los perros albergaban aislados identificados como Staphylococcus spp y el 17% Streptococcus spp. El segundo grupo más numeroso presentaba infecciones por levaduras con M. pachydermatis (44%). La otitis externa debida a infección por Pseudomonas representó una proporción menor de los casos (12,5%).
Las infecciones observadas representan una muestra representativa de las otitis externas observadas en la práctica, donde el tratamiento puede iniciarse sin el respaldo de los diagnósticos de cultivos microbiológicos disponibles.
Por lo tanto, la combinación de polimixina B, miconazol y prednisolona es una buena elección para el tratamiento de primera línea de la otitis en perros.

An Alivira Group Company
P. I. La Borda Mas Pujades 11-12
P. I. La Borda, Borges Blanques 21-25
08140 Caldes de Montbui
Barcelona (España)
Usar ese formulario solo para consultas de Farmacovigilancia.
Por favor, no usarlo para otros temas.